

CAR T-celtherapie:
De impact van CRS, ICANS en andere bijwerkingen
CAR T-celtherapie heeft de behandeling van verschillende hematologische maligniteiten, waaronder ALL, MM en DLBCL, ingrijpend veranderd en biedt mogelijk veelbelovende resultaten voor deze patiëntengroepen. Hierdoor wordt CAR T-celtherapie niet langer uitsluitend toegepast nadat andere behandelingen niet effectief zijn, maar verschuift deze steeds vaker naar eerdere behandellijnen.
Deze innovatieve therapie gaat echter gepaard met uitdagingen. Bijwerkingen, variërend van mild tot levensbedreigend, kunnen het welzijn van patiënten ernstig beïnvloeden1. Twee van de meest voorkomende en potentieel ernstige bijwerkingen zijn het cytokine release syndrome (CRS) en het immune effector cell-associated neurotoxicity syndrome (ICANS)1. Daarnaast vormen infecties een ander potentieel levensbedreigende complicatie3.
Het zorgvuldig balanceren van effectiviteit en toxiciteit, evenals langdurige monitoring van patiënten, blijft daarom van groot belang. In Nederland werken de CAR T-celtherapiebehandelcentra samen binnen de landelijke CAR T-tumorboard om patiënten die deze behandeling ondergaan optimaal te volgen en te begeleiden.
Het evenwicht tussen toxiciteit en werkzaamheid bij CAR T-celtherapie.
Illustratie van immuun- en CAR T-celactivatie die leidt tot tumorsterfte, CRS en neurotoxiciteit.1
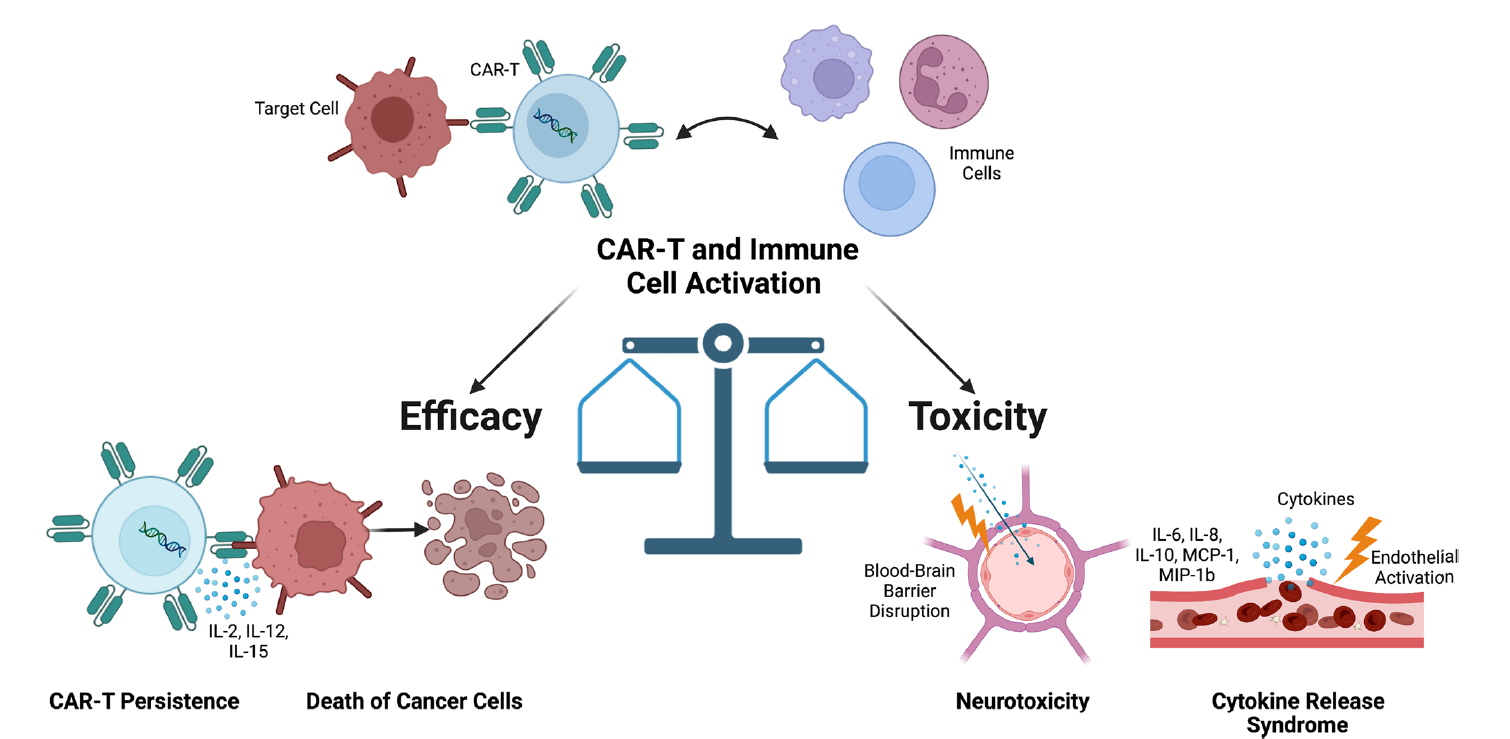
Overgenomen en bewerkt uit: Chohan KL, et al. CAR T cell therapy: the efficacy and toxicity balance. Curr Hematol Malig Rep. 2023 April; 18(2): 9–18. doi:10.1007/s11899-023-00687-7.
IL, interleukin; MCP-1, monocyte chemoattractant protein-1; MIP-1b, macrophage inflammatory protein-1b.
Referenties
1. Chohan KL, et al. CAR T cell therapy: the efficacy and toxicity balance. Curr Hematol Malig Rep. 2023 April; 18(2): 9–18. doi:10.1007/s11899-023-00687-7.
2. Spanjaart AM, et al. The Dutch CAR-T Tumorboard Experience: Population-Based Real-World Data on Patients with Relapsed or Refractory Large B-Cell Lymphoma Referred for CD19-Directed CAR T-Cell Therapy in The Netherlands. Cancer (Basel). 2023. Aug 30;15(17):4334. doi: 10.3390/cancers15174334
3. Haidar G, et al. Infections after anti-CD19 chimeric antigen receptor T-cell therapy for hematologic malignancies: Timeline, prevention, and uncertainties. Curr. Opin. Infect. Dis. 2020, 33, 449–457.
4. Schroeder T, Martens T, Fransecky L, et al. Management of chimeric antigen receptor T (CAR-T) cell-associated toxicities. Intensive Care Med 50, 1459–1469 (2024). https://doi.org/10.1007/s00134-024-07576-4
5. Morris EC, et al. Cytokine release syndrome and associated neurotoxicity in cancer immunotherapy. Nat Rev Immunol. 2022. Feb;22(2):85-96. doi: 10.1038/s41577-021-00547-6.
6. Lee DW, Santomasso BD, Locke FL, et al. ASTCT Consensus grading for cytokine release syndrome and neurologic toxicity associated with immune effector cells. Biol Blood Marrrow Transplant 2019;25:625-38.
7. Hoogland AI, et al. Change in neurocognitive performance among patients with non-Hodgkin’s lymphoma in the first year after CAR T-cell therapy. Transplant Cell Ther. 2022 June ; 28(6): 305.e1–305.e9.
8. Riedel A, et al. Immunological consequences of CAR T-cell therapy: an analysis of infectious complications and immune reconstitution. Blood Adv (2025) 9 (13): 3149-3158. https://doi.org/10.1182/bloodadvances.2024015346
9. Hill JA, et al. How I prevent infections in patients receiving CD19-targeted chimeric antigen receptor T cells for B-cell malignancies Blood. 2020 Jun 24;136(8):925–935. doi: 10.1182/blood.2019004000
10. Johnson PC, et al. Longitudinal patient-reported outcomes in patients receiving chimeric antigen receptor T-cell therapy. Blood Adv (2023) 7 (14): 3541-3550.
11. Abramson JS, et al. Cytokine release syndrome and neurological event costs in lisocabtagene maraleucel-treated patients in the TRANSCEND NHL 001 trial. Blood Adv. 2021 Mar 23;5(6):1695-1705.
12. Azoulay E, et al. Outcomes in patients treated with chimeric antigen receptor T-cell therapy who were admitted to intensive care (CARTTAS): an international, multicentre, observational cohort study. Lancet Haematol. 2021;8:e355-64.
13. Bangol, A, et al. Comprehensive Review of Early and Late Toxicities in CART-Cell Therapy and Bispecific Antibody Treatments for Hematologic Malignancies. Cancers 2025, 17, 282. https://doi.org/10.3390/ cancers17020282
NO-NL-2500026
 icon below, scroll down and tap 'Add to Homescreen'.
Click 'Add' to install the app on your iPad.
icon below, scroll down and tap 'Add to Homescreen'.
Click 'Add' to install the app on your iPad.