
Immunologische gevolgen van CAR T-celtherapie
Infecties
Infecties worden vastgesteld bij 23% tot 42% van de patiënten die een CAR T-celtherapie ondergaan.3 Door de veranderingen in het immuunsysteem die deze behandeling met zich meebrengt, hebben patiënten een verhoogd risico op infecties, met name bacteriële en virale, vooral in de eerste maanden na de therapie.8,9 Hoewel het infectierisico na verloop van tijd afneemt, kunnen er nog steeds ernstige infecties optreden en kunnen sommige patiënten langdurige immuunstoornissen ontwikkelen.8,9
Fasen van opportunistische infecties bij ontvangers van anti-CD19 CAR T-celtherapie.9
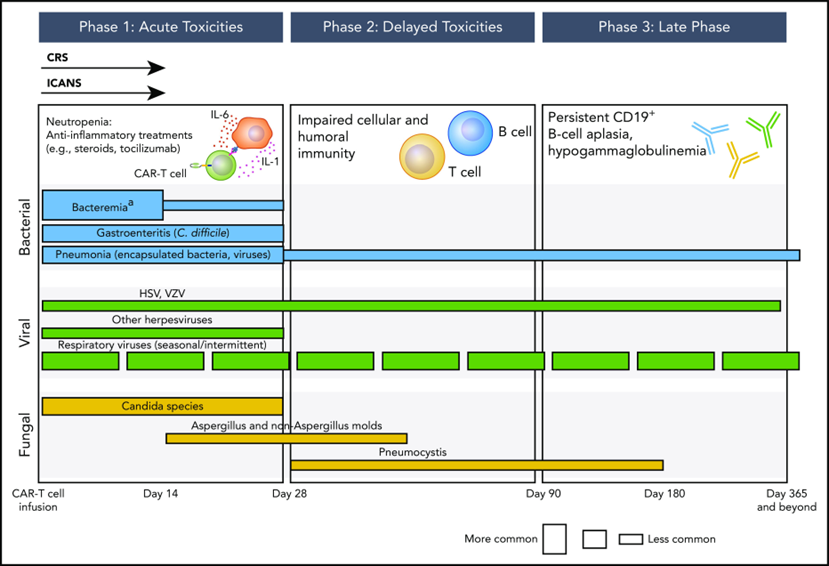
Overgenomen uit: Hill JA, et al. How I prevent infections in patients receiving CD19-targeted chimeric antigen receptor T cells for B-cell malignancies Blood. 2020 Jun 24;136(8):925–935. doi: 10.1182/blood.2019004000
B-cel depletie
CAR T-celtherapie kan leiden tot een aanzienlijke en soms aanhoudende afname van B-cellen, een type witte bloedcellen.8 Dit kan patiënten kwetsbaarder maken voor infecties, vooral in de eerste maanden na de behandeling.3
Hypogammaglobulinemie
Hypogammaglobulinemie is een ernstige bijwerking na een CAR T-celtherapie en wordt toegeschreven aan de vernietiging van B-cellen door de anti-CD-19 CAR T-cellen.8 De hypogammaglobulinemie geeft een verhoogd risico op opportunistische infecties.4 IgG waarden worden daarom gemonitord en indien noodzakelijk wordt substitutie van IgG gegeven.
Langdurige Cytopenie
Cytopenieën, met name neutropenie, trombocytopenie en anemie, zijn veelvoorkomende bijwerkingen na CAR T-celtherapie.8 Deze cytopenieën kunnen vroeg optreden, binnen de eerste paar weken, of laat, na een maand of langer.3,8
Referenties
1. Chohan KL, et al. CAR T cell therapy: the efficacy and toxicity balance. Curr Hematol Malig Rep. 2023 April; 18(2): 9–18. doi:10.1007/s11899-023-00687-7.
2. Spanjaart AM, et al. The Dutch CAR-T Tumorboard Experience: Population-Based Real-World Data on Patients with Relapsed or Refractory Large B-Cell Lymphoma Referred for CD19-Directed CAR T-Cell Therapy in The Netherlands. Cancer (Basel). 2023. Aug 30;15(17):4334. doi: 10.3390/cancers15174334
3. Haidar G, et al. Infections after anti-CD19 chimeric antigen receptor T-cell therapy for hematologic malignancies: Timeline, prevention, and uncertainties. Curr. Opin. Infect. Dis. 2020, 33, 449–457.
4. Schroeder T, Martens T, Fransecky L, et al. Management of chimeric antigen receptor T (CAR-T) cell-associated toxicities. Intensive Care Med 50, 1459–1469 (2024). https://doi.org/10.1007/s00134-024-07576-4
5. Morris EC, et al. Cytokine release syndrome and associated neurotoxicity in cancer immunotherapy. Nat Rev Immunol. 2022. Feb;22(2):85-96. doi: 10.1038/s41577-021-00547-6.
6. Lee DW, Santomasso BD, Locke FL, et al. ASTCT Consensus grading for cytokine release syndrome and neurologic toxicity associated with immune effector cells. Biol Blood Marrrow Transplant 2019;25:625-38.
7. Hoogland AI, et al. Change in neurocognitive performance among patients with non-Hodgkin’s lymphoma in the first year after CAR T-cell therapy. Transplant Cell Ther. 2022 June ; 28(6): 305.e1–305.e9.
8. Riedel A, et al. Immunological consequences of CAR T-cell therapy: an analysis of infectious complications and immune reconstitution. Blood Adv (2025) 9 (13): 3149-3158. https://doi.org/10.1182/bloodadvances.2024015346
9. Hill JA, et al. How I prevent infections in patients receiving CD19-targeted chimeric antigen receptor T cells for B-cell malignancies Blood. 2020 Jun 24;136(8):925–935. doi: 10.1182/blood.2019004000
10. Johnson PC, et al. Longitudinal patient-reported outcomes in patients receiving chimeric antigen receptor T-cell therapy. Blood Adv (2023) 7 (14): 3541-3550.
11. Abramson JS, et al. Cytokine release syndrome and neurological event costs in lisocabtagene maraleucel-treated patients in the TRANSCEND NHL 001 trial. Blood Adv. 2021 Mar 23;5(6):1695-1705.
12. Azoulay E, et al. Outcomes in patients treated with chimeric antigen receptor T-cell therapy who were admitted to intensive care (CARTTAS): an international, multicentre, observational cohort study. Lancet Haematol. 2021;8:e355-64.
13. Bangol, A, et al. Comprehensive Review of Early and Late Toxicities in CART-Cell Therapy and Bispecific Antibody Treatments for Hematologic Malignancies. Cancers 2025, 17, 282. https://doi.org/10.3390/ cancers17020282
NO-NL-2500026
 icon below, scroll down and tap 'Add to Homescreen'.
Click 'Add' to install the app on your iPad.
icon below, scroll down and tap 'Add to Homescreen'.
Click 'Add' to install the app on your iPad.